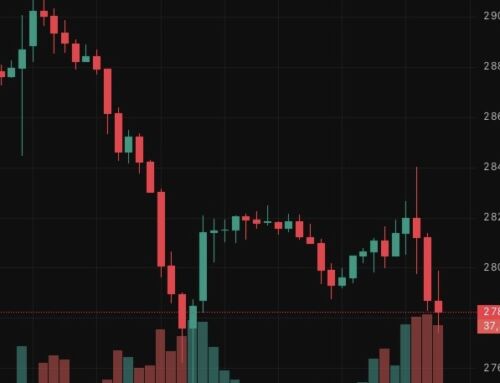
L’Or et la cyanuration (ou cyanurisation de l’or)
l est le procédé le plus couramment utilisé pour l’extraction de l’or. La production de réactifs pour le traitement des minerais pour récupérer l’or, le cuivre, le zinc et l’argent représente environ 13% de la consommation de cyanure dans le monde, les 87% restants du cyanure étant utilisé dans d’autres procédés industriels tels que les plastiques, les adhésifs et les pesticides. En raison de la nature très toxique du cyanure, le processus est controversé et son utilisation est interdite dans un certain nombre de pays et territoires.
En 1783, Carl Wilhelm Scheele a découvert que l’or se dissous dans les solutions aqueuses de cyanure. Grâce au travail de Bagration (1844), Elsner (1846), et Faraday(1847), il a été déterminé que chaque atome d’or requis deux molécules de cyanure, dans l’équilibre et la proportion du composé soluble (stœchiométrie).
Processus industriel
John Stewart MacArthur a développé le procédé de cyanure pour l’extraction de l’or en 1887.L’expansion des mines d’or dans la région du Rand en l’Afrique du Sud a commencé à ralentir dans les années 1880, et puis des nouveaux gisements ont été trouvé mais sous une forme de minerai de pyrite. L’or ne pouvait pas être extrait de ce genre de minerai avec les procédés et les technologies chimiques disponibles.
En 1887, John Stewart MacArthur, a travaillé en collaboration avec les frères Robert et William Forrest pour la Société Tennant à Glasgow, en Ecosse, ils ont développé le procédé « Mac Arthur-Forrest » pour l’extraction de l’or des minerais. En suspendant le minerai broyé dans une solution de cyanure, une séparation de jusqu’à 96-97 % d’or pur a été obtenue, nettement supérieur que par les techniques par gravité de cette époque qui donnait un rendement de 65-70 % d’or récupéré.
Le processus a été utilisé pour la première sur le Rand en 1890, conduisant à un boom de l’investissement et de plus grandes mines d’or ont été alors ouvertes.En 1896, Bodländer a confirmé que l’oxygène était nécessaire dans le processus, quelque chose qui avait été mis en doute par MacArthur, et il a découvert que le peroxyde d’hydrogène était formé comme un intermédiaire.
Les réactions chimiques de l’or
La réaction chimique pour la dissolution de l’or, « l’équation Elsner » est comme suit:
Au 4 + 8 NaCN + O 2 + 2H 2 O → Na 4 [Au (CN)2] +4 NaOH
Dans ce procédé redox, l’oxygène enlève, par l’intermédiaire d’une réaction en deux étapes, un électron de chaque atome d’or pour former le complexe Au (CN) -2. Ion
Méthode et application
Le minerai d’or est réduit en une fine poudre en utilisant des concasseurs et des broyeurs à boulets. Selon le minerai, il est parfois concentré avant par flottation par moussage ou par concentration centrifuge (gravité).
L’eau est ajoutée pour produire une bouillie ou pâte. Le minerai en suspension alcaline peut être combiné avec une solution de cyanure de sodium ou le cyanure de potassium, soit le nombre des opérations utilisent le cyanure de calcium, qui est plus rentable.
L’or est ensuite récupéré en ajoutant des copeaux de zinc ou d’aluminium dans la solution du sel quadruple.
2Na (Au(CN)2) + Zn à Na2(Zn(CN)4) + 2 Au
La solution est ensuite acidifiée avec de l’acide sulfurique pour éliminer l’excès de zinc, séchée et passée dans un four à 800 °C en présence d’air pour oxyder le plomb, le fer et le zinc. Le résidu après une première fonte contient 80-90 % d’or.
Pour éviter la création de toxique du cyanure d’hydrogène au cours du traitement, de la chaux éteinte (hydroxyde de calcium) ou de la soude (hydroxyde de sodium) est ajoutée à la solution d’extraction pour assurer que l’acidité au cours de cyanuration qui est maintenue au-dessus d’un pH a 10,5 -. Fortement alcaline le nitrate de plomb peut améliorer le lessivage de l’or en vitesse et en quantité récupérée, en particulier dans le traitement de minerais partiellement oxydés.
Effet de l’oxygène dissous
L’oxygène est l’un des réactifs consommés pendant la cyanuration, et une déficience en oxygène dissous ralentit le taux de lixiviation.
L’Air ou le gaz d’oxygène pur peuvent être injectés à travers la pâte de minerais afin de maximiser la concentration de l’oxygène dissous. Ce qui a pour effet d’augmenter la pression partielle de l’oxygène en contact avec la solution, la concentration en oxygène dissous est bien supérieur au niveau de saturation qu’à la pression atmosphérique.
L’oxygène peut également être ajouté par dosage de la pâte avec du peroxyde d’hydrogène en solution.
Pré-aération et lavage du minerai d’or
Dans certains minerais, en particulier ceux qui sont partiellement sulfurisé, l’aération (avant l’introduction de cyanure) du minerai dans l’eau à un pH élevé peut rendre éléments tels que le fer et le soufre moins réactif au cyanure, rendant ainsi le procédé de cyanuration plus efficace.
Plus précisément, l’oxydation du fer en oxyde de fer (III) et puis précipitation comme hydroxyde de fer réduit au minimum la perte de cyanure à partir de la formation de complexes de cyanure ferreux. L’oxydation du composé soufre en sulfate évite la consommation de cyanure.
Récupération de l’or à partir de solutions de cyanure
Dans l’ordre décroissant de l’efficacité économique, les processus communs pour la récupération de l’or solubilisée dans la solution sont (certains des processus peuvent être exclus de l’utilisation par des facteurs techniques):
- Par filtration dans le charbon actif puis extraction de l’or
- Par électrolyse ou électro extraction
- Par le processus Merrill-Crowe – un système complexe de filtration et de décantation à contre-courant
Processus d’assainissement des cyanures dans les mines d’or.
Les différentes espèces de cyanure qui restent dans les flux de résidus des mines d’or sont potentiellement toxiques, et sur certaines des opérations des déchets sont traitées par un processus de désintoxication avant leurs rejets. Cela réduit les concentrations des composés de cyanure, mais ne l’élimine pas complètement dans les déchets. Les deux principaux processus utilisés sont le processus sous licence INCO et le procédé à l’acide de Caro. Les deux procédés utilisent des oxydants pour oxyder le cyanure en cyanate, ce qui est aussi toxique que l’ion cyanure, et qui peut ensuite réagir pour former des carbonates et de l’ammoniac:
CN -+ [O] → OCN -OCN -+ 2 H 2 O → HCO – 3 + NH 3
Le processus Inco peut généralement réduire les concentrations de cyanure en dessous de 50 mg / L, alors procédé à l’acide de Caro peut réduire les niveaux de cyanure à entre 10 et 50 mg / L, avec les faibles concentrations en solution réalisable flux plutôt que des suspensions. Le peroxyde d’hydrogène et de chloration alcaline peuvent également être utilisé, bien que ceux-ci soient généralement moins communs.
Un des autres oxydants pour la dégradation des cyanures qui a été d’attirer l’intérêt industriel est l’acide de Caro – un acide peroxomonosulfurique ou persulfurique qui est un puissant oxydant (H 2 SO 5).
L’acide de Caro convertit le cyanure en cyanate. Le Cyanate s’hydrolyse dans l’eau puis s’associe des ions ammonium et carbonate. Le procédé à l’acide de Caro est capable de baisser les niveaux de cyanure en dessous de 50 mg / L, ce qui est généralement adapté à décharge à résidus. Généralement, la meilleure application de ce procédé est avec des résidus de boues contenant des niveaux initiaux de faible à modérée de cyanure et lorsque les niveaux de cyanure a atteindre de de moins d’environ 10 à 50 mg / L sont obligatoires.
Plus de 90 mines dans le monde entier utilisent maintenant un circuit de désintoxication Inco SO 2 / air pour convertir le cyanure en cyanate qui beaucoup moins toxique avant que les déchets soient déversés dans un bassin a résidus.
Typiquement, ce processus on souffle de l’air comprimé à travers les résidus lors de l’ajout de méta bisulfite de sodium qui libère SO 2, le sulfate de cuivre est ajouté comme catalyseur si il n’y a pas suffisamment de cuivre dans l’extrait de minerai. Cette procédure peut réduire les concentrations de «l’acide faible dissociables » de cyanure au-dessous de 10 ppm exigés par la directive sur les déchets miniers de l’UE.
Effets sur l’environnement
En dépit d’être utilisé dans la production de 90% des mines d’or, la cyanuration de l’or est controversée en raison de la nature toxique de cyanure. Bien que les solutions aqueuses de cyanure se dégradent rapidement a la lumière du soleil, les produits moins toxiques, tels que les cyanates et thiocyanates peuvent persister pendant plusieurs années. Des catastrophes célèbres ont tué quelques personnes – les populations doivent être averties de ne pas boire l’eau ou d’aller près de l’eau polluée – mais déversements de cyanure peuvent avoir un effet dévastateur sur les rivières, tout tuant et polluant parfois pendant plusieurs kilomètres en aval. Toutefois, le cyanure est vite lavé des systèmes fluviaux et, aussi longtemps que les organismes peuvent migrer dans des zones non polluées en amont, les zones touchées peuvent être rapidement repeuplées.
Bien que le cyanure ne soit pas cher, efficace et biodégradable, sa haute toxicité a conduit à de nouvelles méthodes pour extraire l’or en utilisant des réactifs moins toxiques. L’utilisation des concentrateurs centrifuge par gravité accrue permettre soit de l’évité, soit de réduire considérablement les volumes de minerai à traité.
En Afrique, il y a beaucoup de projets de retraitements des déchets miniers issus de l’orpaillage par les deux méthodes associées.